Междисциплинарный подход в профилактике и коррекции нежелательных явлений противоопухолевой терапии
Гематологические осложнения наблюдаются у большинства пациентов, получающих химиотерапию. Наиболее частое из них это нейтропения. При продолжительной нейтропении 3-4 степени может развиться фебрильная нейтропения(ФН). При ФН частота летальных исходов по разным данным достигает 10 - 15%. Этой проблеме была посвящена встреча онколога д.м.н., проф. Антона Владимировича Снегового и иммунолога д.м.н. Людмилы Юрьевны Гривцовой.
А.В. Снеговой отметил, что при назначении химиотерапии, большинство онкологов стараются следовать общим принципам соблюдения доз и режима введения на протяжении всего курса. Однако, известно, что в случае развития нейтропении 3-4 степени редукция доз и удлинение интервалов между курсами являются вынужденной мерой профилактики ФН. Как показал опрос 64 онкологов, 41 % респондентов не проводят оценку риска развития нейтропении до начала химиотерапии и столько же предпочитают модифицировать режимы ХТ – редуцировать дозу, увеличивать интервалы между курсами в случае развития гематологической токсичности. «Необходимо проведение оценки риска развития ФН у каждого пациента до начала химиотерапии», - подчеркнул эксперт. При оценке риска учитывают как режим химиотерапии, так и индивидуальные характеристики пациента. Полный алгоритм оценки риска ФН представлен в клинических рекомендациях Общества специалистов поддерживающей терапии в онкологии (RASSC) (ссылка доступна после авторизации).
Онколог подробно представил современные возможности проведения профилактики ФН препаратами из группы Г-КСФ (гранулацитарного колониестимулирующего фактора). Как известно, существуют непегилированные (для ежедневного введения) и пегилированные (для однократного введения на курс с интервалом не менее 14 дней) формы препаратов. Главное преимущество пэг-Г-КСФ - механизм рецептор-опосредованного протеолиза, позволяющий молекуле циркулировать в крови до тех пор, пока не восстановится абсолютное число нейтрофилов (АЧН). А.В. Снеговой напомнил, что важно начинать профилактику ФН в первые 24-72 часа после химиотерапии!
Не рекомендовано вводить Г-КСФ в день проведения химиотерапии, т.к. это повышает риск развития ФН в течение последующих курсов, пневмонии, тромбоцитопении! Не стоит также вводить Г-КСФ во время лучевой терапии на область грудной клетки, средостения из-за увеличения частоты случаев супрессии костного мозга. Следует прекратить введение Г-КСФ как минимум за 48 часов до введения химиотерапии.
Л.Ю. Гривцова рассказала о возможностях применения иммуномодуляторов в профилактике ФН. Иммунотропные препараты применяются как для профилактики иммуносупрессивного влияния самой опухоли, так и для коррекции иммунодефицитных состояний, вызванных применением химиотерапии. Включение в режимы иммунотропных препаратов, считает иммунолог, приведет к повышению эффективности специфического лечения и более полной реализации намеченной схемы.
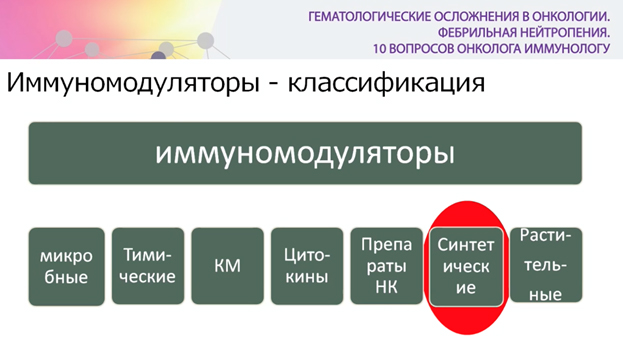
Более подробно Л.Ю. Гривцова остановилась на синтетических иммуномодуляторах. По ее словам, механизм их воздействия на организм лучше изучен и предсказуем. К синтетическим препаратам относятся низкомолекулярные (галавит, гепон, глутаксим) и высокомолекулярные (азоксимера бромид). Азоксимера бромид – препарат отечественного производства с показанием к применению в комплексной терапии у взрослых пациентов:
- после химио- и лучевой терапии, хирургического удаления опухоли (длительное применение) для профилактики иммунодепрессивного влияния опухоли, коррекции иммунодефицита;
- до и на фоне химиотерапии для снижения иммунодепрессивного, гепато- и нефротоксического действия цитостатиков.
Иммунолог представила результаты российского исследования с включением 96 пациенток с диагнозом РМЖ. Пациентки были распределены в группы «контроль» и «азоксимера бромид». Исследование показало, что в группе «азоксимера бромид» нейтропения 3 ст. наблюдалась реже, а 4 ст. не регистрировалась по сравнению с контрольной группой. Л.Ю. Гривцова подробно описала механизм действия препарата, который обладает гемостимулирующей и гемопротективной активностью, обеспечивает защиту нейтрофилов от действия цитостатиков. При этом эксперт подчеркнула необходимость его комплексного применения с другими препаратами, в том числе с Г-КСФ для профилактики тяжелой миелосупрессии.
Все ли пациенты должны получать иммунокоррегирующую терапию?
Нет, не все. Иммунокоррегирующая терапия показана тем пациентам, которые получают высокотоксичную терапию с необходимостью сохранения дозоинтенсивности (больные раком молочной железы, яичников, легкого, пациенты, получающие препараты платины), пациенты, которым предстоит большое оперативное вмешательство.
Обязательно ли выполнять исследование иммунного статуса перед назначением иммуномодуляторов?
В большинстве случаев проведение такого исследования с последующей консультацией врача-иммунолога необходимо. «Основной принцип назначения иммунотропной терапии – оценка состояния пациента. Мы предполагаем, что онкологический пациент иммуноскомпрометирован, но какое звено иммунитета повреждено у конкретного больного, мы не можем знать. Пациентам с диагнозом рак молочной железы, рак легкого желательно включать иммуномодулирующие препараты в стандартные схемы, при этом, проводить оценку иммунного статуса не обязательно. А вот в случае рака яичников, иммунологическое исследование, по мнению Л.Ю. Гривцовой, имеет принципиальное значение.
Есть ли предпосылки для сочетания иммуномодуляторов с таргетными препаратами и противоопухолевой иммунотерапией?
По словам Л.Ю. Гривцовой, пока таких исследований не проводилось, но потенциал у такой комбинированной терапии есть. Наибольший интерес в плане изучения представляет активация азоксимером бромидом экспрессии рецепторов, которые ответственны за воздействие этих противоопухолевых препаратов.
Стоит ли применять азоксимера бромид у больных солидными опухолями с метастатическим поражением костного мозга?
Предпосылки для этого есть: препарат продемонстрировал эффективность у пациентов с онкогематологическими заболеваниями с поражением костного мозга.
Есть ли рациональное зерно в идее иммунореабилитации пациентов после завершения лечения по поводу онкологического заболевания?
«Для онкологических пациентов необходимо рассматривать возможности реабилитации на всех этапах лечения. Если мы будем проводить профилактику до назначения иммуносупрессивной противоопухолевой терапии или проведения обширных хирургических вмешательств, ранних и отсроченных осложнений будет гораздо меньше. И это тема последующих исследований. Я за иммунореабилитацию, которая включает целый комплекс мероприятий, но, повторю, начинать нужно как можно раньше», - поделилась Л.Ю. Гривцова.
Профилактика фебрильной нейтропении в клинической практике онколога
д.м.н. Антон Владимирович Снеговой
Возможности использования иммуномодуляторов в профилактике фебрильной нейтропении
д.м.н. Людмила Юрьевна Гривцова
Дискуссия. 10 вопросов онколога иммунологу



