Междисциплинарный подход в профилактике и коррекции нежелательных явлений противоопухолевой терапии
Вакцинация онкологических больных - тема, которая вызывает большой интерес и в то же время, много опасений, как у самих пациентов, так и у врачей. Что важно знать о вакцинации взрослых пациентов? Могут ли вакцины стимулировать рост злокачественных опухолей или влиять на ход лечения основного заболевания? Какие ожидать нежелательные иммунные реакции? Есть ли абсолютные противопоказания для вакцинации онкологических больных? Эти вопросы обсуждали главный инфекционист Минздрава России проф. Владимир Петрович Чуланов и онколог к.м.н. Николай Юрьевич Соколов.
Прежде всего, профессор В.П. Чуланов остановился на общих принципах вакцинопрофилактики и напомнил слушателям: применение живых вакцин не допустимо для пациентов, проходящих химио-, лучевую терапию. Если же есть необходимость такой вакцинации, то она должна быть проведена не позднее, чем за 1 месяц до начала иммуносупрессивной терапии, и не ранее, чем через 3 месяца после ее окончания.
|
Корь, краснуха, паротит |
Вакцинация возможна спустя 3 мес. после терапии |
|
Ветряная оспа |
Вакцинация возможна спустя 3-12 мес. после терапии |
|
Ротавирусная инфекция |
Вакцинация не рекомендуется, но возможна спустя 3 мес. после терапии |
|
Желтая лихорадка |
Вакцинация возможна спустя 3-6 мес. после терапии |
Данные ограничения связаны с риском развития вакциноассоциированных заболеваний. Инактивированные вакцины (это могут быть рекомбинантные, белковые, векторные, ДНК-, РНК- вакцины и другие, главная их особенность – они созданы не на основе живого возбудителя) более предпочтительны для пациентов с онкологическими заболеваниями. Однако и эти вакцины не рекомендуют применять во время курсов иммуносупрессивной терапии (исключение составляют экстренная вакцинопрофилактика гепатита B и сезонные прививки против гриппа). Сами по себе инактивированные вакцины не опасны для пациента, но из-за подавления различных звеньев иммунного ответа необходимый протективный иммунитет может не сформироваться. Для достижения максимального иммунного ответа такие прививки целесообразно вводить за 2 недели до начала или спустя 3 месяца после окончания иммуносупрессивной терапии.
|
Столбняк, коклюш, дифтерия, гемофильная инфекция типа b (Хиб-инфекция), менингококковая инфекция, ВПЧ, гепатит А |
Вакцинация возможна спустя 3 мес. после терапии |
|
Гепатит B |
Возможна вакцинация спустя 3 мес. после начала терапии. Экстренная вакцинопрофилактика возможна во время лечения |
|
Пневмококковая инфекция |
Пациентам, которые ранее не вакцинировались против превмококковой инфекции, рекомендуется ввести 1 дозу 13-валентной вакцины, а затем 1 дозу 23-валентной вакцины через 8 недель |
|
Грипп |
Вакцинация возможна до начала эпидемического сезона с учетом соотношения польза/риск |
Как видно из приведенной таблицы, через 3 месяца после завершения лучевой, цитостатической терапии возможно использование большинства вакцин. Если речь идет о лечении препаратами антител к B-клеткам, начало вакцинации рекомендуется не ранее, чем через 6 мес.
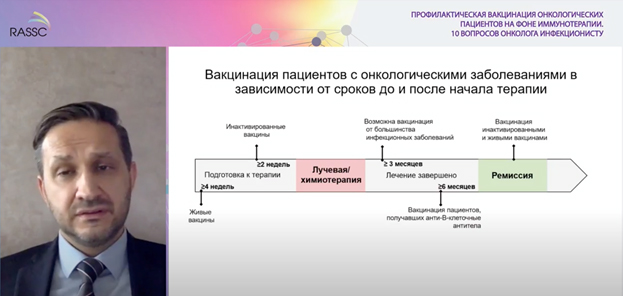
В период ремиссии вакцинация проводится в соответствии с рекомендациями для здоровых взрослых.
Онколог Н.Ю. Соколов привел данные Американского общества инфекционных болезней (IDSA) и Европейской конференции по инфекциям при лейкемии (ECIL), которые рекомендуют ежегодную вакцинацию противогриппозной вакциной. Исключение составляет интенсивная терапия, например, индукционная или консолидирующая терапия острых лейкозов. При пандемии гриппа среди онкологических пациентов формируется защитный ответ.
Конечно же всех интересует, эффективность и безопасность вакцины против COVID-19 у онкологических больных. Но пока не накоплено достаточно знаний об этом. Все данные, на которые опираются экспертные онкологические общества, заимствуют из опыта вакцинации от гриппа. По словам Соколова, медицинское сообщество с осторожностью высказывает предположения о том, что у пациентов, получающих противоопухолевое лечение, возникает защитный ответ с помощью вакцин против COVID-19. Мы видим, что смертность среди онкологических пациентов, инфицированных COVID-19, выше по сравнению с общей смертностью от онкологических заболеваний. Наиболее актуальным был вопрос о влиянии COVID-19 на пациентов, получающих ингибиторы контрольных точек иммунного ответа (ИКТ). Онколог продемонстрировал результаты мультицентрового исследования с участием 110 пациентов в возрасте от 27 до 86 лет из 19 клиник США, Европы и Австралии. Цель исследования - выяснить, является ли ИКТ дополнительным риском тяжелого течения COVID-19 у онкологических больных. 58 % участников исследования получали лечение по поводу меланомы, 16 % - по поводу НМРЛ, 9 % - ПКР. 85 % получали анти-PD-1 или анти-PD-L1 терапию, 15 % - анти-CTLA-4 – анти-PD-1 терапию, 15 % получали кортикостероиды для коррекции НЯ, 23 % ранее получали химиотерапию. Среди основных симптомов были отмечены лихорадка, кашель, одышка. У 62 % пациентов симптомы отсутствовали. Н.Ю. Соколов подчеркнул особую сложность в дифференциации нежелательных явлений (НЯ) иммунотерапии и признаков вирусной пневмонии. НЯ иммунотерапии могут напоминать инфекционные: общая слабость, миалгия, иногда лихорадка, одышка и кашель. 32 % пациентов были госпитализированы, большая часть прекратила терапию ИКТ. 46 % умерли во время госпитализации.
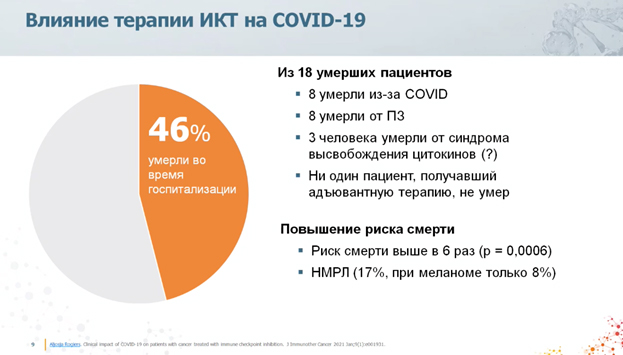
Авторы исследования проанализировали факторы, которые ассоциировались с госпитализацией. К ним относились комбинированная иммунотерапия и использование глюкокортикоидов ≥ 10 мг. Смертность была на порядок выше у людей, которые получали терапию непосредственно с паллиативной целью. Среди «более легких» пациентов, которые получали адъювантную терапию, смертности не было.
На сегодня, данные о вакцинации от COVID-19 на фоне терапии ингибиторами контрольных точек иммунного ответа очень ограничены. Онколог представил проспективные данные о 23 пациентах с НМРЛ (публикация 2018 года), которым проводили вакцинацию от гриппа во время применения ингибиторов PD-1. Вакцинация обеспечивла серологическую защиту, но повышала риск иммуноопосредованных НЯ. Самое главное, подчеркнул эксперт, что в этом исследовании была доказана эффективность вакцинации. Есть основания предполагать, что и при вакцинопрофилактике COVID-19 пациенты будут получать защитную реакцию.
Без внимания не остались вопросы вакцинации на фоне таргетной терапии. Онколог с осторожностью высказал несколько заключений, которые «нуждаются в более длительном подтверждении»:
- таргетная терапия в большинстве случаев не вызывает иммуносупрессию, но может оказывать непреднамеренное ингибирующее воздействие на функцию антигенпрезентирующих клеток, активацию Т-клеток и сигнализацию В-клеток;
- у пациентов, которые получали таргетную терапию, такую как сунитиниб или сорафениб, развивается серопротекция вакциной против гриппа, и она сопоставима со здоровыми контрольными группами;
- не выявлено различий в серопротекции против гриппа при сравнении контрольной группы (больные раком молочной железы, получавшие трастузумаб).
В свою очередь В.П. Чуланов сообщил, что живых вакцин против COVID-19 в России и в мире нет. Инфекционист подробно остановился на характеристиках векторных вакцин. «Многие слышали, что векторные вакцины создают на основе вирусных векторов. Например, «Спутник» создан на основе аденовируса человека 5 и 26 типа. Но мы не называем эту вакцину живой. Аденовирус, который используется в данной вакцине, является генетически измененным. Это аденовирус, который лишен генов, отвечающих за размножение. Он не способен размножаться, попадая в клетку, он доносит туда фрагмент гена коронавируса для того, чтобы формировался защитный иммунитет. Поэтому мы относим векторную вакцину к неживым, и ее можно применять у пациентов с онкологическими заболеваниями», - рассказал В.П. Чуланов.
Особые указания в инструкциях к вакцинам против COVID-19 в отношении пациентов с онкологическими заболеваниями
|
Название вакцины |
С осторожностью |
Противопоказания |
|
Гам-КОВИД-Вак |
Злокачественные новообразования |
- |
|
ЭпиВакКорона |
Вторичный иммунодефицит |
Злокачественный иммунодефицит |
|
КовиВак |
- |
- |
Профессор Чуланов пояснил, что особые рекомендации в инструкциях к «Гам-КОВИД-Вак» и «ЭпиВакКорона» связаны с недостаточностью данных о безопасности. Производители вакцины «ЭпиВакКорона» внесли злокачественные новообразования в раздел противопоказаний, поэтому данный препарат у онкологических пациентов не применяют. Для вакцины «КовиВак» никаких противопоказаний нет, использовать ее необходимо по аналогии с другими инактивированными вакцинами.
Эксперты подробно ответили на вопросы, которые слушатели присылали заранее и задавали в чате вебинара.
Есть ли у онкологических пациентов противопоказания к вакцинации? И какая из отечественных вакцин лучше?
Наличие противопоказаний в инструкциях не означает, что были получены какие-то данные, что эта вакцина неэффективна или может негативно повлиять на развитие основного заболевания. В целом все три отечественные вакцины с точки зрения безопасности при использовании у онкологических больных одинаковы.
Но правильнее будет применять «Спутник V» или «КовиВак», поскольку в инструкции к этим препаратам нет противоопказаний к применению у онкологических больных. Опыт применения этих вакцин, особенно «Спутника», достаточно большой, и никаких серьезных побочных эффектов, в том числе у пациентов с онкологическими заболеваниями, не наблюдалось.
Не стоит также пренебрегать и вакцинацией «окружению» пациента («коконная вакцинация»).
Может ли вакцинация стимулировать рост злокачественной опухоли?
Что касается вакцин против COVID-19, таких эпидемиологических исследований не проводилось. Но исследования в отношении других вакцин на протяжении большого периода времени таких рисков не показали. По словам В.П. Чуланова, «не стоит преувеличивать значимость вакцины, как некоего фактора, который кардинальным образом нарушает работу иммунной системы. Наш организм постоянно сталкивается с новыми антигенами. Введение вакцины - это встреча с еще одним антигеном, и ожидать от этого экстраординарного влияния на развитие опухолевого заболевания оснований нет».
Есть ли абсолютные противопоказания для вакцинации у онкологических пациентов?
Они те же самые, что и у обычных пациентов:
- наличие в анамнезе тяжелых иммунных реакций на использование вакцин (анафилактический шок, отек квинке и др. жизнеугрожающие реакции);
- беременность;
- возраст младше 18 лет.
ESMO рекомендует использовать вакцины против COVID между курсами химиотерапии. Стоит ли это делать, учитывая короткие сроки «отдыха» между курсами: 1-3 недели?
Сама химиотерапия не является противопоказанием к вакцинации неживыми вакцинами. Единственное, чего можно опасаться: не удастся достичь желаемого эффекта. Как отметил В.П. Чуланов, «за 1-3 недели полноценного восстановления функций иммунной системы не происходит. Но у определенного процента пациентов можно ожидать формирования защитного иммунитета. Поэтому проведение вакцинопрофилактики в промежутках между химиотерапией допустимо. Если говорить о трехнедельном перерыве, лучше это делать в самой середине между курсами лекарственной терапии». Н.Ю. Соколов также поддержал собеседника, но предостерег слушателей, что вакцинация в данной ситуации допустима, если нет выраженной гематологической токсичности, каких-либо НЯ.
Может ли вакцинация против COVID-19 на фоне ИКТ индуцировать цитокиновый шторм?
«Убедительных научных данных, которые могли бы ответить на этот вопрос, пока нет. На сегодня вакцинированы сотни миллионов пациентов в мире, в нашей стране более 20 миллионов. В этом пуле пациентов люди с разным иммунным статусом, и ни у одного человека не было зафиксировано такого НЯ как развитие цитокинового шторма. С моей точки зрения оснований ожидать такой реакции при использовании ингибиторов контрольных точек нет», - высказал свое мнение В.П. Чуланов.
Известно, что даже практически здоровые лица по-разному переносят вакцину: в некоторых случаях развивается гриппоподобный синдром, миалгия, повышается температура. Может ли вакцинация против COVID-19 усугубить общее состояние больного в период восстановления после полихимиотерапии?
«Уже есть опыт использования вакцин у пациентов как в процессе, так и после окончания всех курсов химиотерапии. Речь идет о пациентах, которые были в адъювантном режиме. Конечно, усугубление состояния возможно. Более того, пациенты, которые переносили терапию с гематологической либо с какой-то другой токсичностью, восстанавливаются в большинстве случаев после вакцинации тяжелее. Необходимо пациентов предупреждать об этом. И как мы говорили с моим коллегой, чем больше перерыв до начала противоопухолевой терапии или после, тем лучше переносится вакцина. Прививка в процессе лечения – это исключительно вынужденная мера, на которую мы идем, выбирая меньшее из зол», - подчеркнул Н.Ю. Соколов.
В некоторых публикациях были сообщения о том, что вакцинация «Спутником V» больше двух инъекций невозможна. Может ли «Спутник V» индуцировать аутоиммунные заболевания? Можно ли прививаться «Спутником» повторно, например, через год?
«Возможность или невозможность повторного использования вакцины «Спутник V» связана с другим, - пояснил В.П. Чуланов. - Вектором является аденовирус человека. С аденовирусами мы все постоянно сталкиваемся. Наличие антител может привести к тому, что вакцина инактивируется нашим собственным иммунитетом. С этим и было связано рассуждение, что, скорее всего, повторная вакцинация будет неэффективна. Но это теоретические рассуждения. Практика показывает, что иммунитет, сформировавшийся к аденовирусам, приблизительно через полгода угасает и не имеет сильного влияния на вектор, содержащийся в вакцинном препарате. Поэтому ревакцинация вполне возможна. Пока просто непонятно, необходимо это или нет.
Что касается развития аутоиммунных заболеваний, никаких доказательств, что данные вакцины способствуют развитию аутоиммунных процессов нету. Аутоиммунный процесс – реакция на собственные антигены, и в данном случае вакцина не является каким-то особым стимулятором иммунной системы. Никаких антигенов, сходных с антигенами человеческого организма, она не содержит».
Нужно ли вакцинироваться пациентам, перенесшим COVID-19, у которых выявлен низкий титр IgG?
Нет, не нужно. Данных о целесообразности вакцинации после перенесенной инфекции на сегодняшний день нет.
Почему вакцинированные с высоким уровнем антител люди болеют COVID?
Как пояснил В.П. Чуланов, ни одна вакцина не работает на 100%. Есть небольшая доля людей, у которых не формируется тот протективный иммунитет, который должен формироваться как после перенесенного заболевания, так и после вакцинации. В этом случае мы вполне можем ожидать повторного заболевания даже при инфицировании тем же самым штаммом вируса. Кроме того, вирус постоянно меняется, и исключить нечастые случаи повторного заражения мы не можем. Но относительно общего количества вакцинированных и переболевших доля таких случаев невысока.
Главный инфекционист также призвал онкологов и других специалистов внимательнее относиться к понятию «уровень антител». Чаще всего используют качественные/неколичественные тест-системы, которые показывают лишь пограничное значение оптической плотности: выше определенного значения «+», ниже «-». Эти данные нельзя использовать как количественную оценку уровня, или титра антител.
Можно ли рассчитывать на изобретение вакцины от рака?
«Я очень позитивно смотрю на будущее вакцинологии, - заявил В.П. Чуланов. – Есть вакцины профилактические, есть терапевтические. И в той, и в другой областях уже есть достижения. Примеры эффективных вакцин, которые предотвращают развитие злокачественных новообразований: против ВПЧ, против вируса гепатита В. Когда мы будем лучше понимать патогенез заболеваний, мы сможем сделать еще больше.
Но уже появляются вакцины для лечения онкологических заболеваний, направленные против конкретных антигенов раковых клеток, которые отличают их от здоровых, помогают иммунной системе находить очаги и бороться с ними».
Вакцинация онкологических пациентов. Что важно знать
профессор Владимир Петрович Чуланов
Взгляд онколога на вопросы вакцинации онкологических пациентов
к.м.н. Николай Юрьевич Соколов
Дискуссия. 10 вопросов онколога инфекционисту


