Междисциплинарный подход в профилактике и коррекции нежелательных явлений противоопухолевой терапии
17 декабря 2020 г. состоялся вебинар «Иммуноопосредованные гепатиты. 10 вопросов онколога гепатологу». Это второй вебинар из цикла научно-образовательных мероприятий «Мультидисциплинарный подход к коррекции нежелательных явлений в онкологии».
Д.м.н., проф. Марина Викторовна Маевская, гепатолог, гастроэнтеролог, главный научный сотрудник научно-исследовательского отдела инновационной терапии Первого МГМУ им. И.М. Сеченова, зам. директора по лечебной работе Клиники пропедевтики внутренних болезней, гастроэнтерологии и гепатологии им. В.Х. Василенко, и Александр Николаевич Юрченков, врач отделения химиотерапии больницы № 62, представили точки зрения гепатолога и онколога на проблему иммуноопосредованных гепатитов.
Иммунотерапия применяется практически при всех злокачественных опухолях. Однако, при активации Т-клеток на фоне терапии анти CTLA-4 и PD-(L)1 могут развиться иммуноопосредованные нежелательные явления (ИО НЯ). Эти реакции неспецифичны и могут затрагивать любые органы и системы. У большинства пациентов ИО НЯ развиваются в первые 3 месяца лечения. Гепатит занимает одно из лидирующих мест среди НЯ иммунотерапии.
Ведущие вебинара подчеркнули важность междисциплинарного взаимодействия онкологов, гепатологов и гастроэнтерологов.
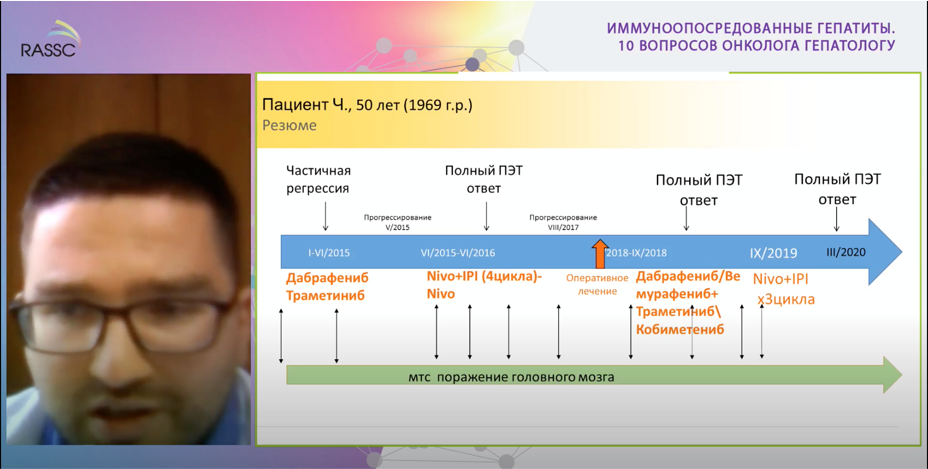
А.Н. Юрченков поделился уникальным случаем из своей клинической практики лечения пациента с рецидивом меланомы кожи, метастазами в почку, надпочечник и головной мозг. Пациенту была назначена комбинированная иммунотерапия ниволумаб + ипилимумаб. Лечение осложнилось развитием аутоиммунного гепатита. Успешное купирование нежелательного явления позволило провести 7 циклов иммунотерапии и добиться полного опухолевого ответа несмотря на распространенность заболевания.
Александр Николаевич акцентировал внимание слушателей на некоторых важных моментах, которые необходимо выполнить до начала иммунотерапии для снижения риска иммуноопосредованного гепатита:
- Оценить наличие аутоиммунного заболевания в анамнезе (аутоиммунное заболевание не является абсолютным противопоказанием к терапии, но есть риск его обострения);
- Анализы на ВИЧ, HCV, HBV, ЦМВ;
- Биохимический и клинический анализ крови и анализы на гормоны щитовидной железы (ТТГ, Т3, Т4);
- Провести беседу с пациентом о возможных НЯ, о необходимости сообщить доктору о появлении первых симптомов НЯ.
Профессор М.В. Маевская подробно остановилась на вопросах дифференциальной диагностики аутоиммунного и вирусного гепатитов, особенно HBV. Эксперт обратила внимание на необходимость использования важного маркера - антитела к HBcore-антигену вируса гепатита В. По ее словам, у пациентов с иммуносупрессией высока вероятность реактивации скрытой инфекции. И в этих случаях, возможно, потребуется специфическое лечение.
Гепатологи назначают выполнение анализа на HBcore антиген всем пациентам с подозрением на гепатит. Марина Викторовна обратила особое внимание на предосторожности, связанные с проведением противовирусной терапии гепатита С. Почему это так важно? При инфицировании двумя вирусами лечение HCV может реактивировать скрытую инфекцию HBV и привести к развитию фульминантного гепатита. Профессор Маевская указала на сходство данной реакции с ИО гепатитом. Гепатолог считает, что определение антител к HB-core антигену необходимо ввести в рутинную клиническую практику онкологов, которые назначают иммунотерапию или иммуносупрессивное лечение.
Существуют ли предикторы ИО поражения печени? Есть ли еще какие-то лабораторные маркеры, которые стоит дополнительно посмотреть перед началом иммунотерапии? По данным экспертов вебинара, таких маркеров пока не найдено.
Александр Николаевич отметил, что гепатит может развиться как при моно-, так и на фоне комбинированной иммунотерапии. Он указал на то, что при назначении комбинированной иммунотерапии интервал времени до начала клинических симптомов НЯ, которые могут привести к летальному исходу, составляет всего 14 дней. Таким образом, если режим введения комбинированной иммунотерапии – 1 раз в 3 недели, то НЯ могут развиться уже после первого введения. Поэтому необходимы мониторинг анализов и коммуникация с пациентом, особенно на первых курсах лечения, для своевременной оценки возникающих у него проблем. Чаще гепатотоксичность имеет бессимптомное течение и единственным индикатором являются лабораторные показатели. При их появлении необходимо, как было сказано выше, исключить вирусные гепатиты и метастатическое поражение печени. При подтверждении связи гепатита с иммунотерапией назначают кортикостероиды. В случаях резистентного течения необходимо рассмотреть назначение иммуносупрессоров (микофенолата мофетил или такролимус). В свою очередь, профессор Маевская настоятельно не рекомендовала таким пациентам назначать Инфликсимаб в связи с высоким риском инфекционных осложнений.
Важным моментом дискуссии между онкологом и гепатологом было обсуждение алгоритмов ведения пациентов в зависимости от степени тяжести поражения печени. Профессор М.В. Маевская обратила внимание на необходимость индивидуального подхода к каждому конкретному пациенту. «Я не предлагаю игнорировать инструкции, но призываю к большой осторожности при назначении высоких доз преднизолона пожилым, коморбидным пациентам, людям в плохом физическом состоянии, - рекомендовала профессор Маевская. – Если речь идет о средней или тяжелой степени гепатотоксичности, и врач назначает преднизолон или метилпреднизолон, то количество побочных эффектов может «конкурировать» с эффективностью. Назначение больших доз преднизолона может, в частности, вызвать гипергликемию». В этом случае специалист допускает возможность отказа от кортикостероидов и начала терапии препаратами 2-й линии.
Также гепатолограссказала об алгоритмах ведения пациентов с легкой степенью токсичности. «Если у пациента легкая степень токсичности, бессимптомное повышение АСТ и АЛТ, то в соответствии с рекомендациями можно продолжать терапию, не корректируя ее, - отметила М.В. Маевская. – Но онкологи, терапевты, как правило, стоят перед искушением назначить что-то из гепатопротекторов. Не стоит спешить, не стоит их использовать для лечения в случаях, когда есть только изменения лабораторных показателей. Повышение уровня АЛТ и АСТ в 5-10 раз обычно пугает онкологов. Но если у пациента нормальный билирубин, и он не предъявляет жалоб, не нужно волноваться. Лучше использовать больше времени на диагностику возникшего патологического состояния. Опасным является повышение уровня билирубина. Билирубин и факторы коагуляции напрямую отражают синтетическую функцию печени». Специалист напомнила о законе Хая (Hy’s law) – важном прогностическом методе, который помогает предсказать неблагоприятный исход лекарственного поражения печени в случае одновременного повышения билирубина и сывороточных трансаминаз.

Нужно ли при подозрении на аутоиммунный гепатит проводить биопсию печени? Эксперты сошлись во мнении, что эту процедуру необходимо выполнять только в том случае, если есть сомнения в диагнозе, или в рамках научных исследований.
В заключение эксперты обсудили очень волнующий онкологов вопрос - какие клинические рекомендации являются наиболее предпочтительными для коррекции осложнений, связанных с печенью? Были отмечены руководства Санкт-Петербургского общества гастроэнтерологов, гепатологов и диетологов, Санкт-Петербургского гепатологического общества, Российского общества по изучению печени (РОПИП), Общества специалистов по поддерживающей терапии в онкологии (RASSC), Российского общества клинической онкологии (RUSSCO), Европейской ассоциации по изучению печени (EASL).
В 2021 г. RASSC продолжит серию мультидисциплинарных встреч, дискуссий, посвященных коррекции нежелательных явлений в онкологии. Следите за нашими новостями.



